Merit Medical HepaSphere Microspheres(With Doxorubicin) IFU-Int'l: FRANÇAIS
FRANÇAIS: Merit Medical HepaSphere Microspheres(With Doxorubicin) IFU-Int'l

730095003_A ID 102412_IFU HS DOXO :print 9/11/12 17:07 Page 7
FRANÇAIS
vasculaire et après examen de l’angiographie artérioveineuse.
U
TILISATION PREVUE :
• Du fait des complications importantes liées à une mauvaise
Les Microsphères HepaSphere™ sont indiquées pour une utilisation
embolisation, une prudence extrême doit être appliquée pour de
dans l'embolisation de vaisseaux sanguins avec ou sans administration
q
uelconques interventions impliquant une circulation extracrânienne
de chlorhydrate de doxorubicine à des fins thérapeutiques ou pré-
englobant la tête et le cou, et le médecin doit sérieusement peser les
o
pératoires dans les interventions suivantes :
bienfaits potentiels du recours à l’embolisation par rapport aux risques
•
Embolisation du carcinome hépatocellulaire
et aux complications potentiels de la procédure. Ces complications
• Embolisation de métastases hépatiques
p
euvent comprendre la cécité, une perte auditive,la perte de l'odorat, la
paralysie et la mort.
DESCRIPTION
• Le patient peut développer de graves lésions cutanées inhérentes à
Les Microsphères HepaSphere appartiennent à une classe d'agents
l’irradiation du fait de longues périodes d'exposition à l'angiographie, en
e
mboliques basés sur des technologies brevetées. Elles sont conçues
c
as de forte corpulence, d’incidences obliques, de séries répétées
pour une embolisation contrôlée et ciblée. Les Microsphères HepaSphere
d
'enregistrement d'images ou de radiographies multiples. Se reporter
peuvent être chargées en chlorhydrate de doxorubicine et sont capables
au protocole clinique de votre établissement pour vous assurer que la
de libérer le médicament localement dans la zone d'embolisation. Les
dose d'irradiation correcte est utilisée pour chaque type de procédure
Microsphères HepaSphere sont biocompatibles, hydrophiles, non
réalisée.
résorbables, expansibles et déformables. Les Microsphères HepaSphere
• L’apparition de lésions par irradiation chez le patient peut être
gonflent quand elles sont mises en contact avec des solutions aqueuses.
retardée. Les patients doivent être informés des effets potentiels des
Elles sont disponibles dans différentes tailles.
rayons, de ce qu'il faut rechercher et de la personne à contacter en cas
Sec (µm)
d'apparition de symptômes.
• Les Microsphères HepaSphere NE DOIVENT PAS être reconstituées
30-60
avec de l'eau stérile pour préparation injectable. La reconstitution avec
l'eau stérile entraine un gonflement excessif rendant l'injection des
50-100
Microsphères HepaSphere très difficile, voir impossible.
• Ne pas reconstituer les Microsphères HepaSphere avec du Lipiodol /
100-150
Ethiodol.
150-200
• Apporter une attention particulière aux signes d'embolisation mal
ciblée. Durant l'injection suivre attentivement les signes vitaux du
patient tels que le SAO2 (par exemple, l'hypoxie, les changements du
CONDITIONNEMENT DU DISPOSITIF
SNC). Envisager d'arrêter la procédure,en cherchant un shunt éventuel,
Les Microsphères HepaSphere sont contenues dans un flacon stérile en
ou s'orienter vers une taille de Microsphères supérieure si de
copolymères d'oléfine cyclique (COC) de 10 ml, muni d'une capsule
quelconques signes de mauvais ciblage se produisent ou si le patient
sertie et placé dans un sachet scellé.
présente des symptômes.
Contenu : 25 ou 50 mg de Microsphères HepaSphere déshydratées par
• Envisager d'utiliser une taille de Microsphères supérieure si
flacon, à reconstituer avant utilisation.
l'angiographie ne démontre pas rapidement une embolisation évidente
pendant l'injection des Microsphères.
CONTRE-INDICATIONS
• Patients intolérants aux procédures d'obstruction vasculaire
Avertissements
au sujet de l'utilisation de petites microsphères
• Anatomie vasculaire ou flux sanguin empêchant le placement correct
• Une attention toute particulière doit être apportée lorsque les emboles
du cathéter ou l'injection correcte des emboles
ont un diamètre inférieur à la capacité de résolution de votre
• Présence ou suspicion de vasospasme
équipement d'imagerie. La présence d'anastomoses artério-veineuses,
• Présence ou début probable d'une hémorragie
de vaisseaux ramifiés conduisant hors de la zone cible ou de vaisseaux
• Présence d'une maladie athéromateuse sévère
émergents non évidents, peuvent conduire à une embolisation mal
• Artères nourricières trop petites pour accepter les Microsphères
ciblée et à des complications graves.
HepaSphere choisies
• Des microsphères de moins de 100 microns effectueront
• Présence de voies vasculaires collatérales susceptibles de menacer
généralement une migration distale vers les sources anastomotiques et
des territoires sains durant l'embolisation
sont ainsi susceptibles d'emboliser un tissu distal. L'utilisation de
• Shunts artério-veineux à haut débit ou fistules avec un diamètre
microsphères de taille plus petite peut conduire à un risque plus élevé
supérieur à la granulométrie choisie des Microsphères HepaSphere
de lésion ischémique et les conséquences de cette lésion doivent être
• Résistances vasculaires en aval des artères nourricières excluant le
prises en compte avant l'embolisation. Les conséquences potentielles
passage des Microsphères HepaSphere dans la lésion
comprennent le gonflement, la nécrose, la paralysie, un abcès et/ou un
• Présence d'artères alimentant la lésion de taille insuffisante pour
syndrome post-embolisation plus fort.
accepter les Microsphères HepaSphere
• Un gonflement post embolisation peut conduire à une ischémie du
• Utilisation contre-indiquée dans le système vasculaire pulmonaire,
tissu adjacent à la zone cible.Il faut prendresoin d'éviter l'ischémie d'un
coronaire et intracérébral
tissu intolérant, non ciblé tel que le tissu nerveux.
• Sensibilité connue au polyvinylalcool-acrylate de sodium
PRECAUTIONS
AVERTISSEMENTS
Les Microsphères HepaSphere ne doivent être utilisées que par des
• La taille des Microsphères HepaSphere doit être choisie en fonction de
médecins formés aux procédures d'embolisation vasculaire. La taille et
l'aspect angiographique artério-veineux. Les Microsphères HepaSphere
la quantité de microsphères doivent être soigneusement choisies selon
doivent avoir une taille excluant le passage d'une quelconque artère à
la lésion à traiter et la présence éventuelle de shunts. Seul le médecin
une veine.
peut décider du moment le plus approprié pour interrompre l'injection
• Certaines Microsphères HepaSphere peuvent être d’une taille
des Microsphères HepaSphere.
légèrement supérieure à la plage indiquée et le médecin doit donc
Ne pas utiliser si le flacon, le bouchon ou le sachet paraissent
sélectionner avec soin les Microsphères HepaSphere en fonction de la
endommagés.
taille des vaisseaux ciblés au niveau souhaité de l’occlusion du système
7
730095003_A ID 102412_IFU HS DOXO :print 9/11/12 17:07 Page 8
P
our un usage unique – contenu fourni stérile – Ne jamais réutiliser,
i
nférieurs)
r
etraiter ou restériliser le contenu d'un flacon qui a été ouvert. La
•
Une réaction allergique aux médications (par exemple, les
réutilisation, le retraitement ou la restérilisation peuvent compromettre
analgésiques)
l'intégrité structurelle du dispositif et/ou provoquer une défaillance de
• Une réaction allergique aux produits de contraste non ioniques ou aux
c
elui-ci, ce qui à son tour peut entrainer une lésion, une maladie ou le
e
mboles
décès du patient. La réutilisation, le retraitement ou la restérilisation
• La rupture d'un vaisseau ou de la lésion et hémorragie
risquent également de générer une contamination du dispositif et/ou
• La mort
causer une infection ou infection croisée chez le patient, y compris
• Informations supplémentaires disponibles dans la section
notamment, la transmission de maladie(s) infectieuse(s) d'un patient à
Avertissements
l'autre. La contamination du dispositif peut entrainer une lésion, une
m
aladie ou à le décès du patient. Toutes les procédures doivent être
C
OMPORTEMENT DE GONFLEMENT
réalisées selon la technique aseptique acceptée.
Les Microsphères HepaSphere gonflent durant la reconstitution avec une
solution aqueuse de NaCl à 0,9 % et les produits de contraste non
Les Microsphères HepaSphere NE DOIVENT PAS être utilisées
ioniques. Quand elles sont hydratées dans 100 % d'une solution
d
ans leur état sec d'origine.
E
lles doivent être reconstituées avant
a
queuse de NaCl à 0,9 % ou un produit de contraste non ionique, ou 50
l'emploi. Les Microsphères HepaSphere gonflent dans une solution
% de produit de contraste non ionique et 50 % d'une solution aqueuse
aqueuse. L'ampleur du gonflement dépend de la concentration ionique
de NaCl à 0,9 %, les Microsphères HepaSphere gonflent d'environ 4 fois
de la solution. Les microsphères gonflent d'environ quatre fois leur
leur diamètre sec original en environ 10 minutes. Par exemple, des
diamètre sec initial dans une solution aqueuse de NaCl 0,9 % et les
Microsphères HepaSphere ayant un diamètre d'environ 50-100 microns
produits de contraste non ioniques.L'ampleur du gonflement quand elles
à l’état sec gonfleront jusqu'à environ 200-400 microns durant la
sont chargées en chlorhydrate de doxorubicine dépend de la quantité de
reconstitution telle que recommandée ci-dessous.Du fait de la variabilité
médicament avec laquelle le produit est chargé. Le chlorhydrate de
inhérente du processus de gonflement, quelques Microsphères
doxorubicine lyophilisé doit être reconstitué dans une solution de NaCl à
HepaSphere se trouveront légèrement en dehors de cette plage après la
0,9 %. Les Microsphères HepaSphere subissent une légère diminution
reconstitution, de sorte que le médecin doit s'assurer de choisir
de taille d'environ 20 % quand elles sont chargées en chlorhydrate de
soigneusement la taille des Microsphères HepaSphere en fonction de la
doxorubicine par rapport à leur taille dans une solution aqueuse de NaCl
taille des vaisseaux au niveau désiré d’occlusion dans le système
0,9 % pure. Les Microsphères HepaSphere sont compressibles et
vasculaire et en fonction de la nature de la solution aqueuse.
peuvent être injectées facilement à travers des microcathéters.
Note :
Pour gonfler correctement, les Microsphères HepaSphere doivent
Cependant, l'injection des Microsphères HepaSphere avant leur
être exposées à un minimum de 10 ml de solution. L'ampleur du
expansion complète peut les empêcher d'atteindre la cible à emboliser
gonflement, quand il y a chargement en chlorhydrate de doxorubicine,
et provoquer l'embolisation d'une zone tissulaire plus étendue.
dépend de la quantité de médicament avec laquelle le produit est
Note :
La concentration maximale recommandée de chlorhydrate de
chargé. Les Microsphères HepaSphere subissent une légère diminution
doxorubicine est de 5 mg/ml. Les concentrations de chlorhydrate de
de taille d'environ 20 % quand elles sont chargées en chlorhydrate de
doxorubicine supérieures à 5 mg/ml augmentent considérablement la
doxorubicine par rapport à leur taille dans une solution aqueuse de NaCl
viscosité de la solution et rendent le maniement des Microsphères
à 0,9 % pure.
HepaSphere difficile.
COMPATIBILITE AVEC LE CATHETER
Les patients présentant des allergies connues aux produits de contraste
Les Microsphères HepaSphere peuvent être injectées avec des
non ioniques peuvent nécessiter une administration de corticostéroïdes
microcathéters ayant les spécifications suivantes :
avant l'embolisation. Des examens ou précautions supplémentaires
peuvent s'avérer nécessaires pour les soins péri opératoires pour les
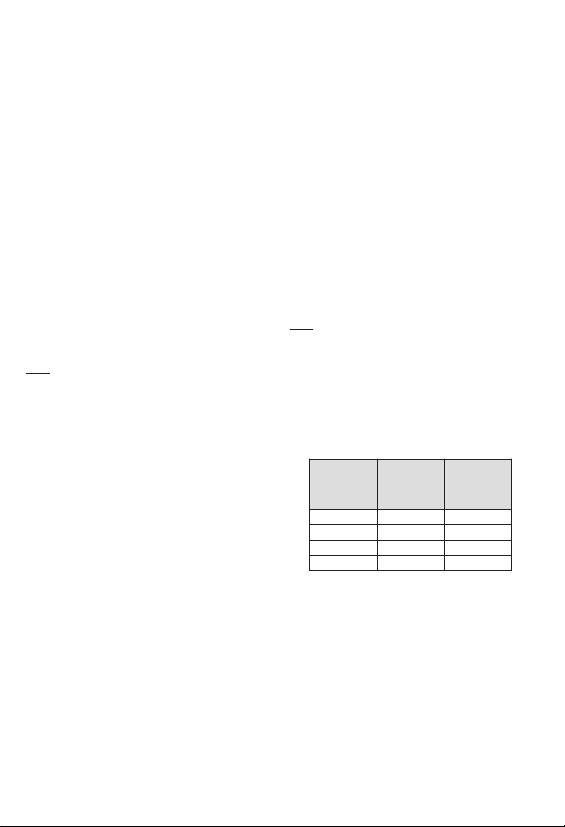
Plage de taille
Diamètre interne
patients atteints des affections suivantes :
reconstituée
Sec (µm)
du cathéter
• Diathèse hémorragique ou état d'hypercoagulabilité
approximative
(pouces)
• Immunodépression
(µm)
30-60 120 - 240
≥ 0.021
COMPLICATIONS POTENTIELLES
L'embolisation vasculaire est une procédure à haut risque. Des
50-100 200 - 400
≥ 0.021
complications peuvent survenir à tout moment pendant ou après
100-150 400 - 600
≥ 0.024
l'intervention et peuvent inclure, mais ne se limitent pas à, ce qui suit :
150-200 600 - 800
≥ 0.027
• Une paralysie résultant d'une embolisation non ciblée ou d'une lésion
ischémique par œdème des tissus voisins
• Un reflux indésirable ou le passage des Microsphères HepaSphere
INSTRUCTIONS
dans les artères saines voisines de la lésion visée ou après traversée de
Les Microsphères HepaSphere doivent être reconstituées avec 100 %
la lésion, dans d'autres artères ou lits artériels, tels que la carotide
d'une solution de NaCl à 0,9 % ou d'un produit de contraste non ionique,
interne, la circulation pulmonaire, ou coronaire
ou avec 50 % de produit de contraste non ionique et 50 % d'une solution
• Une embolie pulmonaire par shunt artério-veineux
aqueuse de NaCl à 0,9 %, en l’absence d’administration de chlorhydrate
• Une ischémie à un endroit non souhaité, comprenant l'accident
de doxorubicine, ou chargées avec une solution de chlorhydrate de
vasculaire cérébral ischémique ou l’infarctus ischémique (y compris
doxorubicine avant le positionnement du cathéter.
l’infarctus du myocarde) et la nécrose tissulaire
• Choisir soigneusement la taille des Microsphères HepaSphere en
• Une occlusion de lit capillaire et une lésion tissulaire
fonction de la taille des vaisseaux au niveau désiré de l'occlusion dans
• Un vasospasme
le système vasculaire et en fonction de la nature de la solution aqueuse.
• Une reperméabilisation
Voir la description « COMPORTEMENT DE GONFLEMENT ».
• la cécité, une perte auditive et la perte de l'odorat
• Des Microsphères HepaSphere peuvent se trouver à l'extérieur du
• Les réactions à un corps étranger nécessitant des soins médicaux
flacon.Aussi,le flacon doit être manié de manière aseptique à l'écart du
• Une infection nécessitant des soins médicaux
champ stérile principal.
• Des complications associées au cathétérisme (par exemple,
• S'assurer de la compatibilité des Microsphères HepaSphere avec le
hématome au point de ponction, formation d'un caillot à l'extrémité du
diamètre du cathéter à utiliser. Voir le tableau ci-dessus.
cathéter et déplacement secondaire ou lésions nerveuses et/ou
• Inspecter l'emballage pour confirmer son intégrité. Retirer le flacon du
vasculaires pouvant entrainer des troubles au niveau des membres
sachet. La surface externe du flacon est stérile.
8

730095003_A ID 102412_IFU HS DOXO :print 9/11/12 17:08 Page 9
d
oxorubicine ne sont pas adaptées au chargement dans les
LES MICROSPHERES HEPASPHERE PEUVENT ETRE UTILISEES
M
icrosphères HepaSphere.
AVEC OU SANS CHARGEMENT EN CHLORHYDRATE DE
D
OXORUBICINE
A
titre d’indication, le chargement du chlorhydrate de doxorubicine
lyophilisé, solubilisé dans une solution de NaCl à 0,9 % dans des
OPTION 1 : PREPARATION POUR UNE EMBOLISATION SANS
Microsphères HepaSphere, prendra une heure. Les Microsphères
CHLORHYDRATE DE DOXORUBICINE
HepaSphere ne doivent pas être utilisées avant d'être complètement
Le temps de reconstitution approximatif quand elles sont utilisées sans
h
ydratées et gonflées. La cinétique de chargement du chlorhydrate de
c
hargement en chlorhydrate de doxorubicine est de 10 minutes.
doxorubicine pré-solubilisé peut varier selon la concentration et le pH de
la solution.
• Remplir une seringue de 10 ml avec 100 % d'une solution aqueuse de
• Choisir la dose appropriée de chlorhydrate de doxorubicine à charger
NaCl à 0,9 % ou un produit de contraste non ionique (ou 50 % de solution
dans les Microsphères HepaSphere.
aqueuse de NaCl à 0,9 % et 50 % de produit de contraste). Connecter la
Note :
s
eringue à une aiguille de calibre égal ou supérieur à 20 G.
U
ne dose maximale de 75 mg de chlorhydrate de doxorubicine peut être
• Pour s'assurer de la reconstitution correcte des Microsphères
chargée dans chaque flacon de Microsphères HepaSphere. Solubiliser la
HepaSphere tenir le flacon horizontalement du bout des doigts et faites
dose souhaitée de chlorhydrate de doxorubicine lyophilisé dans 20 ml
de
rouler le flacon plusieurs fois. Cela fera déposer le contenu sec du flacon
s
olution de NaCl à 0,9 % pour injection. NE JAMAIS UTILISER D'EAU
contre la paroi.
PURE.
Note :
Soulever uniquement la capsule du flacon, sans retirer la bague
Note :
La concentration maximale recommandée de chlorhydrate de
métallique sertie ni le bouchon.
doxorubicine est de 5 mg/ml. Des concentrations de chlorhydrate de
• Introduire soigneusement l'aiguille montée sur la seringue à travers le
doxorubicine supérieures à 5 mg/ml augmentent considérablement la
bouchon du flacon. Continuer à faire rouler le flacon du bout des doigts et
viscosité de la solution et la rendent difficile à manier avec les
injecter le volume total (10 ml) du produit de reconstitution dans le flacon,
Microsphères HepaSphere.
puis positionner le flacon à la verticale et retirer soigneusement
• Aspirer les 20 ml de solution de chlorhydrate de doxorubicine dans
l’ensemble seringue / aiguille.
deux seringues de 30 ml distinctes.Chaque seringue de 30 ml doit donc
Note :
Le flacon est hermétiquement fermé. Des techniques d'aspiration
contenir 10 ml de solution de chlorhydrate de doxorubicine.
et/ou de décompression appropriées, telles qu'approuvées par
• Connecter une des seringues de 30 ml contenant 10 ml de la solution
l'établissement de santé, peuvent être utilisées pour une injection plus
de chlorhydrate de doxorubicine à une aiguille de calibre égal ou
facile du produit de reconstitution dans le flacon. Si de l'air est aspiré du
supérieur à 20 G.
flacon avant la reconstitution, veiller à ne pas faire sortir les microsphères
• Pour s'assurer de la reconstitution correcte des Microsphères
du flacon.
HepaSphere tenir le flacon horizontalement du bout des doigts et faire
• Pour vous assurer d'une reconstitution homogène des Microsphères
rouler le flacon plusieurs fois. Cela fera déposer le contenu sec du flacon
HepaSphere, renverser doucement le flacon par va et vient de sorte que le
contre la paroi.
liquide entre en contact avec le bouchon 5 à 10 fois.
Note :
Soulever uniquement la capsule du flacon, sans retirer la bague
Note :
Une agitation vigoureuse risque de provoquer l'apparition de
métallique sertie ni le bouchon.
microbulles qui peuvent entraîner l'agrégation des microsphères.
• Introduire soigneusement l'aiguille d'une des seringues de 30 ml
• Attendre un minimum de 10 minutes pour laisser les Microsphères
contenant 10 ml de solution de chlorhydrate de doxorubicine à travers le
HepaSphere se reconstituer et gonfler complètement.
bouchon du flacon. Continuer à faire rouler le flacon du bout des doigts
• Utiliser une seringuede 30ml etuneaiguille decalibreégalou supérieur
et injecter la solution complète de 10 ml de solution de chlorhydrate de
à 20G pour aspirer le contenu du flacon.Positionnerle flacon à la verticale,
doxorubicine dans le flacon.
le fond du flaconversle haut.Retirer l'aiguille vers l'arrière de sorte qu'elle
• Positionner le flacon de Microsphères HepaSphere à la verticale.
soit submergée dans le liquide mais pas obturée par le bouchon. Aspirer
Retirer soigneusement la seringue avec l'aiguille attachée, et laisser le
doucement le contenu total du flacon dans la seringue.
flacon reposer durant 10 minutes pour hydrater complètement les
Note :
Si de l‘air a été précédemment aspiré du flacon, une injection
microsphères.
douce d’air en utilisant la seringue avant l’aspiration du contenu du flacon
• Durant la période d'hydratation de 10 minutes, secouer doucement le
assurera une aspiration plus facile du contenu du flacon dans la seringue.
flacon de Microsphères HepaSphere plusieurs fois par va et vient de
Si tout le contenu n’est pas prélevé, introduire un volume supplémentaire
sorte que le liquide entre en contact avec le bouchon gris. Répéter le
d’air et répéter le processus d’aspiration. Il est possible d’ajouter une
processus toutes les 2 à 3 minutes pour assurer une reconstitution
quantité supplémentaire de produit de contraste non ionique ou de
homogène des Microsphères HepaSphere.
solution aqueuse de NaCl à 0,9 % dans la seringue pour obtenir une
Note :
Le flacon est hermétiquement fermé. Des techniques d'aspiration
dispersion plus importante des microsphères.
et/ou de décompression appropriées, telles qu'approuvées par
Note :
Les Microsphères HepaSphere reconstituées comme décrit ci-
l'établissement de santé, peuvent être utilisées pour une injection plus
dessus peuvent être utilisées en présence d'agents chimiothérapeutiques
facile du produit de reconstitution dans le flacon. Si de l'air est aspiré du
tels que le cisplatine, l'épirubicine, le chlorhydrate de doxorubicine, le
flacon avant la reconstitution, veiller à ne pas faire sortir les
fluororacile, l'irinotecan et la mitomycine après hydratation. Cependant
microsphères du flacon.
pour l'administration des médicaments, les Microsphères HepaSphere ne
• Après la période d'hydratation de 10 minutes, connecter une aiguille
sont indiquées que pour une utilisation avec le chlorhydrate de
de calibre égal ou supérieur à 20 G à la seconde seringue de 30 ml
doxorubicine (voir ci-dessous l'option 2).
contenant les 10 ml restants de la solution de chlorhydrate de
• Si les microsphères ont été reconstituées à l’aide d’une solution
doxorubicine et les insérer dans le flacon des Microsphères HepaSphere.
aqueuse de 100 % de NaCl à 0,9 %, un produit de contraste non ionique
Aspirer le contenu du flacon de Microsphères HepaSphere dans la
doit être ajouté dans la seringue contenant les Microsphères HepaSphere
seringue de 30 ml contenant les 10 ml restants de la solution de
pour permettre la visualisation angiographique.Si un produit de contraste
chlorhydrate de doxorubicine. Positionner le flacon à la verticale, le fond
non ionique a été utilisé pour reconstituer les microsphères, il est possible
du flacon vers le haut. Retirer l'aiguille vers l'arrière de sorte qu'elle soit
de rajouter du produit de contraste non ionique.
submergée dans le liquide mais pas obturée par le bouchon. Aspirer
doucement le contenu total du flacon dans la seringue.
OPTION 2 : PREPARATION POUR UNE EMBOLISATION CHARGEE
• Avant de retirer l’aiguille du flacon des Microsphères HepaSphere,tout
EN CHLORHYDRATE DE DOXORUBICINE
en maintenant la seringue à la verticale, tirer doucement sur le piston de
la seringue vers le bas, pour faire sortir la solution qui peut se trouver
AVERTISSEMENT :
les formulations liposomiques de chlorhydrate de
dans le corps de l’aiguille.
9

